研究室リンク
専門分野
神経科学、薬理学
研究概要
ムーンショット目標7「脳内セノインフラメーション」における分担研究「抑うつ・認知症を担うセノインフラメーション病態の脳末梢連関と神経回路の機能・構造変容の解明と医薬品開発への応用」を主導しています。
老化は、抑うつや認知機能障害の発症・進展に関与し、認知症を含むさまざまな脳疾患のリスクを高めます。しかし、その分子・細胞・神経回路レベルのメカニズムには未解明な点が多く残されています。
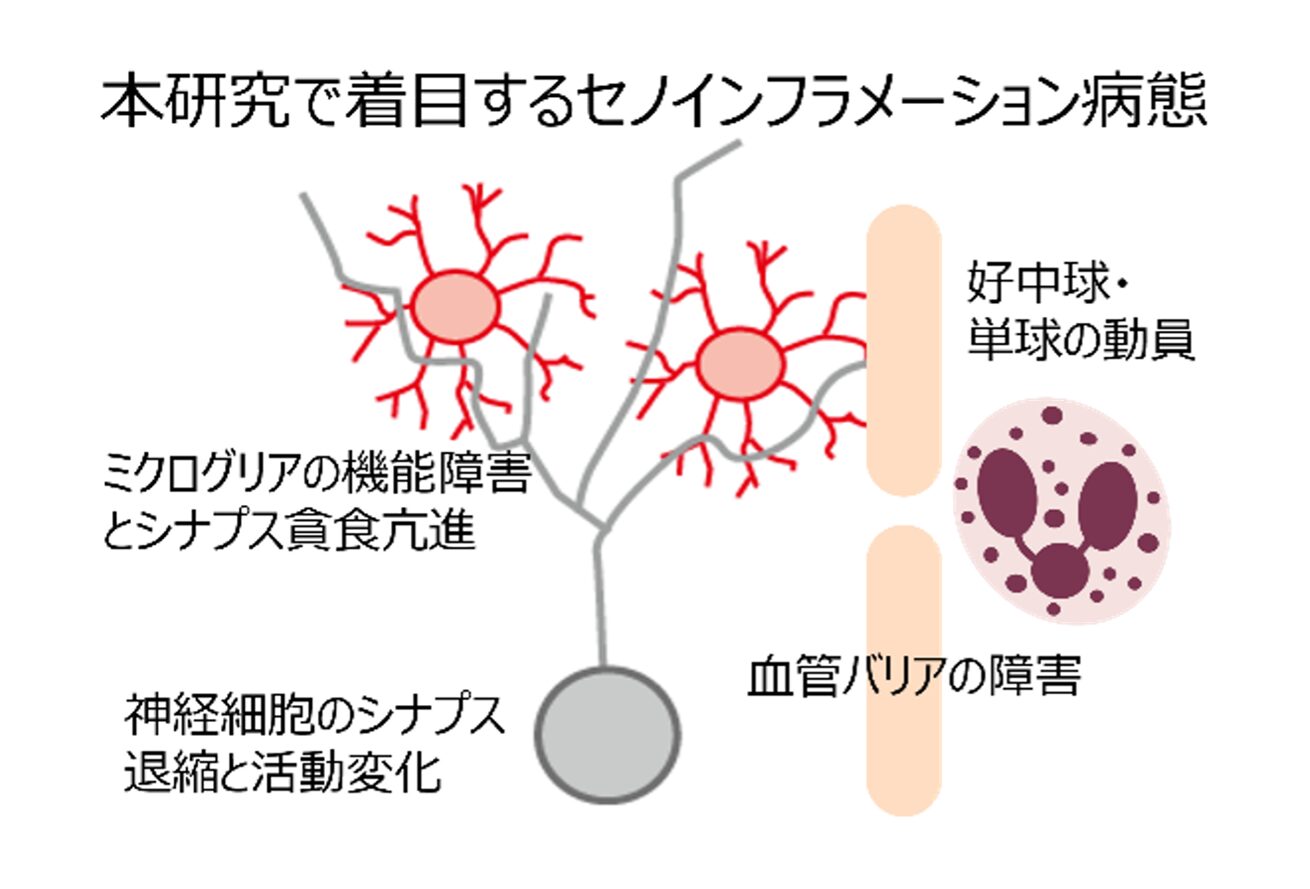
これまで古屋敷らは、慢性ストレスがミクログリアや骨髄由来細胞を起点とする脳・末梢の炎症を介して、神経回路の機能・形態的再編を引き起こし、抑うつや認知機能障害につながることを示してきました。老化に伴い、脳や末梢で炎症関連分子や細胞老化マーカーが増加することが知られていることから、細胞老化と炎症が相互に増幅する状態としてのセノインフラメーションが、老化や認知症に伴う抑うつ・認知機能障害にも関与する可能性があります。一方で、その役割は十分に分かっていません。
本研究では、老齢マウスおよび認知症モデルマウスを用い、多次元行動解析、シングルセル・マルチオミクス解析、全脳イメージングなどの先端手法を組み合わせて、抑うつや認知機能障害に関わる、認知症特有のセノインフラメーション病態を分子・細胞・神経回路レベルで包括的に解明します。さらに、得られたメカニズムを基盤に、認知症の予防・治療のためのバイオマーカー探索や創薬につながる技術基盤を創出します。

主な研究内容
認知症における加齢誘導性セノインフラメーション病態の解明とその可視化・制御技術の創出
認知症をはじめとする神経変性疾患では、加齢が重要な危険因子です。しかし、広く用いられている多くの認知症モデルマウスは、実験上の理由から比較的若齢でも表現型が出やすいよう設計されているため、加齢が認知症発症・進展に果たす役割は十分に解明されていません。
本研究では、まず加齢に伴う脳機能変化(正常老化)を捉え、その分子・細胞・神経回路メカニズムを明らかにします。私たちはこれまでに、老齢マウスでみられる認知機能障害、意欲低下、社会性低下、不安行動の亢進などを幅広く評価できる多次元行動解析基盤を確立してきました。さらに、行動変化ごとに関与する神経回路が異なること、また遺伝的背景によって加齢に伴う行動変化の現れ方が変わることも見出しています。
本研究では、これらの基盤を活用し、全脳イメージングで加齢による行動変容に関わる脳領域を同定し、同定領域における神経活動・神経投射の異常を、電気生理学的手法や組織学的手法で解析し、当該脳領域のセノインフラメーション関連変化を、シングルセル・マルチオミクス解析および空間トランスクリプトーム解析で包括的に評価します。続いて、変化した神経回路・分子の役割を、光・化学遺伝学や分子遺伝学的手法で検証します。並行して、末梢血中の血液細胞の変化も解析し、脳内セノインフラメーション変容との相互関係(脳-末梢連関)を解明します。さらに、遺伝的背景差に着目し、加齢に伴う行動変容の個体差に影響するゲノム要因の解明にも取り組みます。
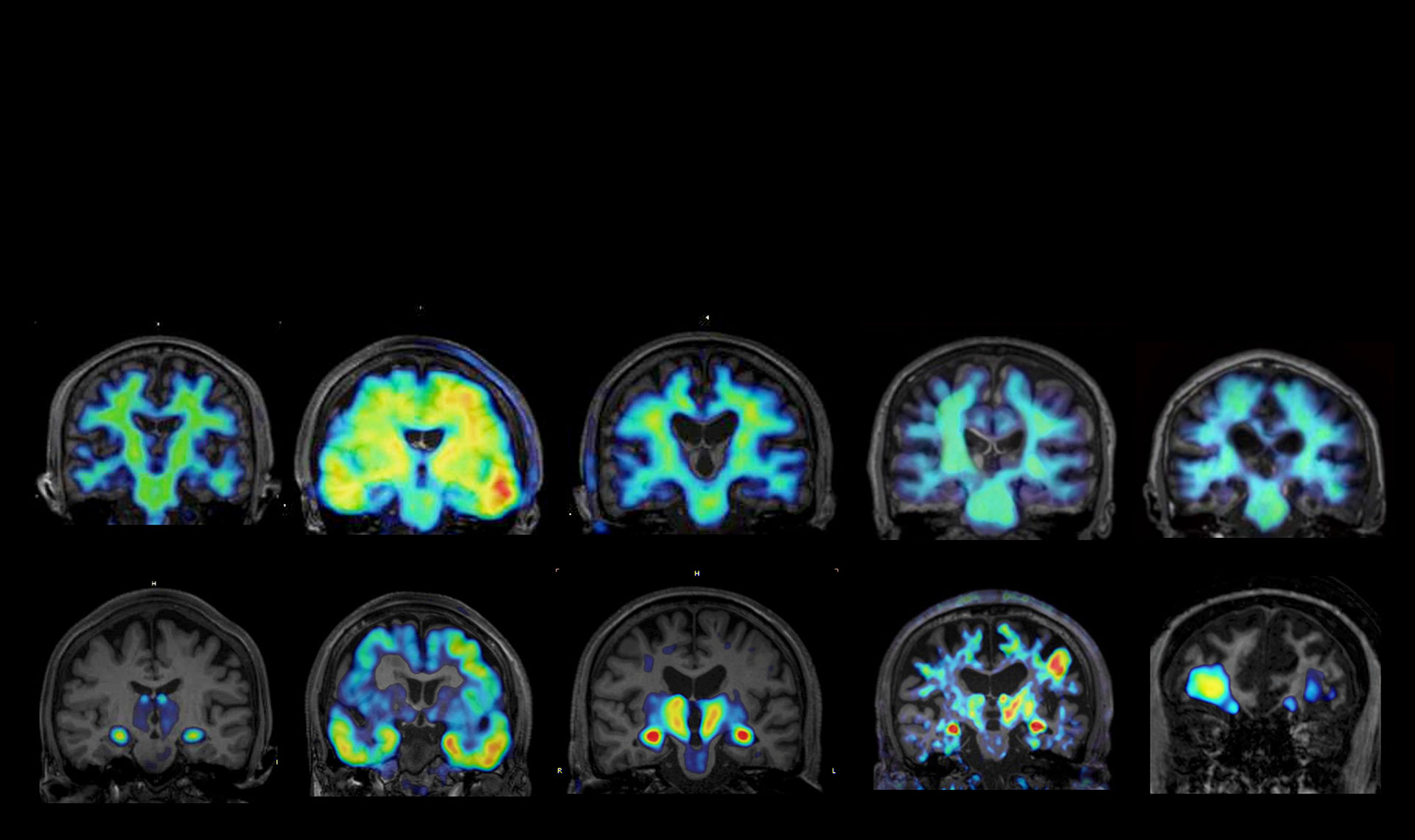
並行して、アミロイドβ変異体やタウ変異体を有する認知症モデルマウスでも同様の解析を行い、正常な脳機能老化と認知症に特異的な加齢誘導性病態の違いを明確化します。これにより、認知症に特有な加齢誘導性のセノインフラメーション病態を抽出します。さらにプロジェクト内外の研究者との共同研究を通じて、軽度認知機能障害・認知症での脳画像研究、血液検体の解析を行うことで、当該病態を標的とした可視化・操作(制御)技術へ展開します。
本研究を通じて、認知症および随伴する精神症状の病態理解を深め、将来的な予防・治療的介入につながる技術基盤の創出を目指します。
研究内容をまとめた総説
Furuyashiki T. Kitaoka S. Neural mechanisms underlying adaptive and maladaptive consequences of stress: Roles of dopaminergic and inflammatory responses. Psychiatry and Clinical Neurosciences 73, 669–675, 2019. doi: 10.1111/pcn.12901
主な論文業績
Okuda Y. Li D. Maruyama Y. Sonobe H. Mano T. Tainaka K. Shinohara R. Furuyashiki T. The activation of the piriform cortex–lateral septum pathway during chronic social defeat stress is crucial for the induction of behavioral disturbances in mice. Neuropsychopharmacology 50, 828–840, 2025. doi: 10.1038/s41386-024-02034-7
Kitaoka S. Tomohiro A. Ukeshima S. Liu K. Wake H. Kimura S.H. Yamamoto Y. Nishibori M. Furuyashiki T. Repeated social defeat stress induces HMGB1 nuclear export in prefrontal neurons, leading to social avoidance in mice. Cells 12, 1789, 2023. doi: 10.3390/cells12131789
Ishikawa Y. Kitaoka S. Kawano Y. Ishii S. Suzuki T. Wakahashi K. Kato T. Katayama Y. Furuyashiki T. Repeated social defeat stress induces neutrophil mobilization in mice: Maintenance after cessation of stress and strain-dependent differences in response. British Journal of Pharmacology 178, 827–844, 2021. doi: 10.1111/bph.15203
Nie X. Kitaoka S. Tanaka K. Segi-Nishida E. Imoto Y. Ogawa A. Nakano F. Tomohiro A. Nakayama K. Taniguchi M. Mimori-Kiyosue Y. Kakizuka A. Narumiya S. Furuyashiki T. The innate immune receptors TLR2/4 mediate repeated social defeat stress–induced social avoidance through prefrontal microglial activation. Neuron 99, 464–479.e7, 2018. doi: 10.1016/j.neuron.2018.06.035
Shinohara R. Taniguchi M. Ehrlich A.T. Yokogawa K. Deguchi Y. Cherasse Y. Lazarus M. Urade Y. Ogawa A. Kitaoka S. Sawa A. Narumiya S. Furuyashiki T. Dopamine D1 receptor subtype mediates acute stress–induced dendritic growth in excitatory neurons of the medial prefrontal cortex and contributes to suppression of stress susceptibility in mice. Molecular Psychiatry 23, 1717–1730, 2018. doi: 10.1038/mp.2017.177