研究室リンク
専門分野
神経免疫学、神経科学
研究概要
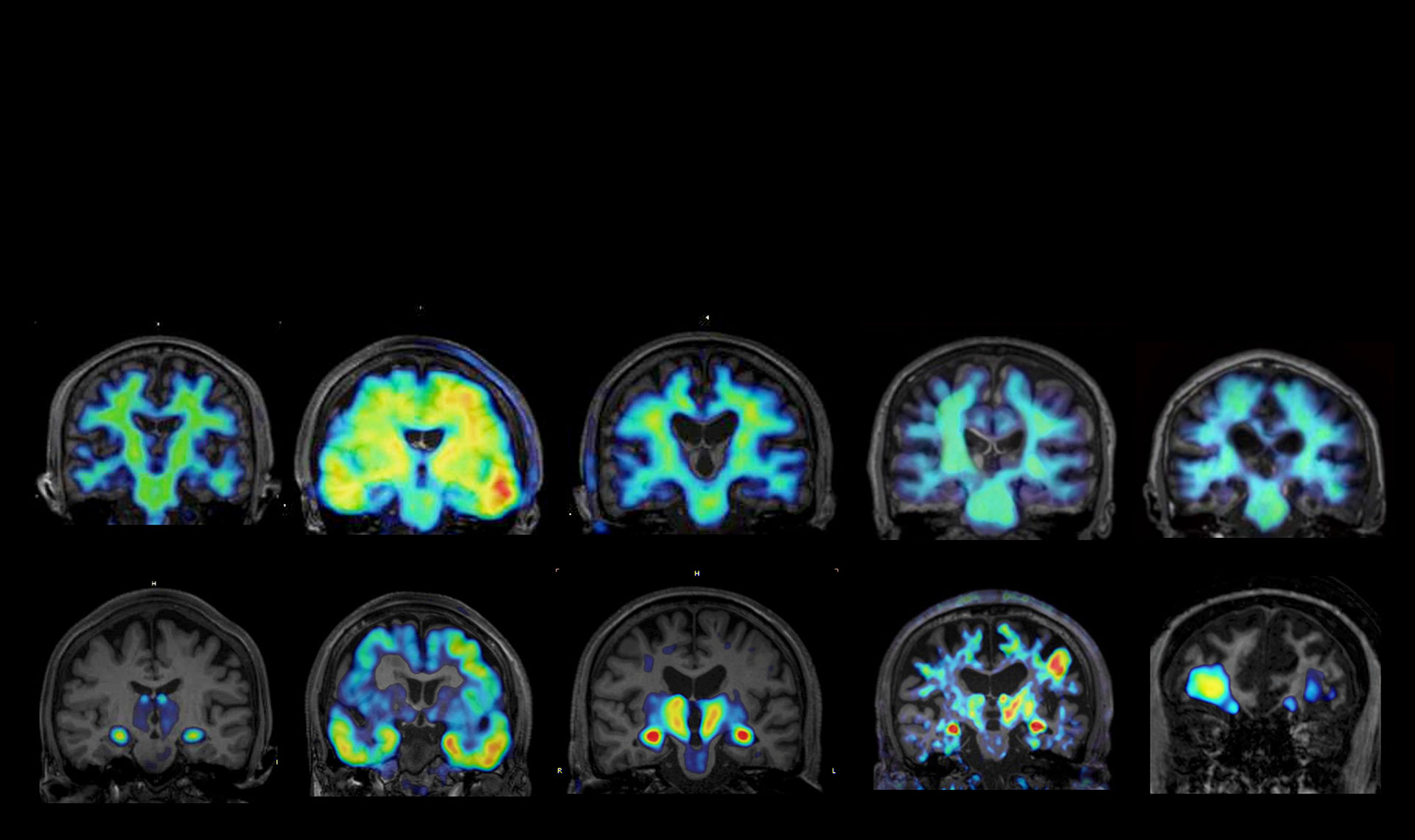
ムーンショット目標7「脳内セノインフラメーション」では、分担項目「高深度マルチオミクス解析を用いた認知症関連病態の総合的解析」を進めています。特に、1細胞空間トランスクリプトーム解析・RNA-seq解析・ATAC-seq解析、網羅的リピドーム解析、エピゲノム解析などを駆使して、老化や慢性炎症に伴うグリア細胞を含めた脳内免疫系と関連した脳実質および脳境界における変容を、細胞個々また多細胞種間、さらには脳境界を含めた領域間や末梢との関係に至る様々なスケールかつ多様なモダリティーで可視化し、脳の機能低下メカニズムを分子・細胞・組織レベルで統合的に解析・理解し、認知症の早期発見や介入方法の創出と検証を進めます。
主な研究内容
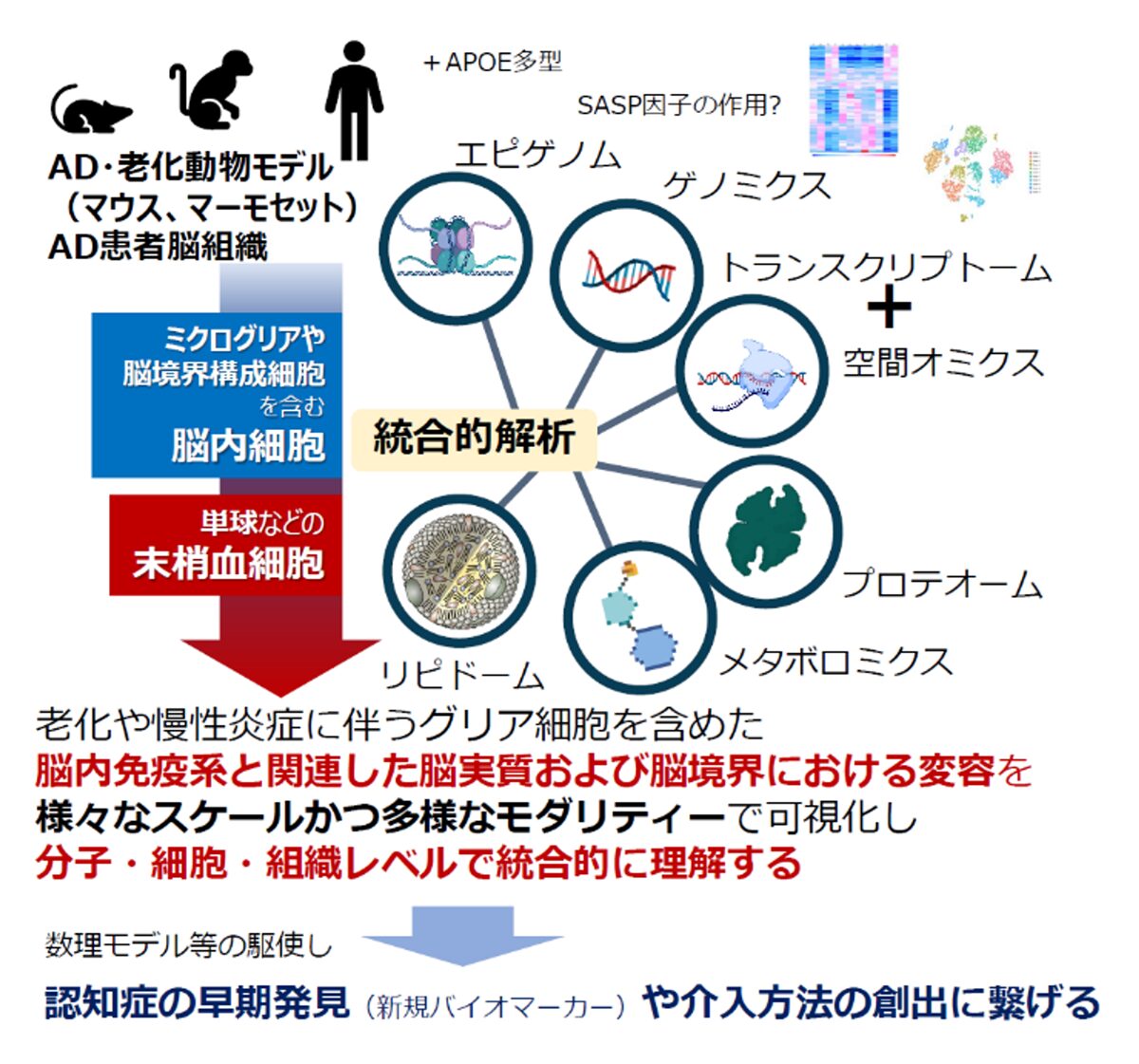
マルチオミクス解析を用いた老化や慢性炎症に関連する脳実質の器質的変容の同定
複雑かつ高度な中枢機能を担う脳は、様々な外的・内的因子による影響を受けながらも、多種細胞間の双方向性の相互作用によってその機能が厳密に維持・制御されています。そのため、認知症に至る脳の機能低下メカニズムを理解するためには、多次元かつマルチスケールな脳内情報を統合的に解析することが必要不可欠であると考えます。そこで私たちは、老化や慢性炎症に伴うグリア細胞を含めた脳内免疫系と関連した脳実質および脳境界における変容を、全脳透明化や高深度なマルチオミクス解析などの最先端解析技術を用いて多様なモダリティーで可視化し、脳の機能低下メカニズムを分子・細胞・組織レベルで統合的な解析を進めています。
脳実質および境界を標的とした脳機能低下メカニズムの解明と介入技術の開発
認知症の病態メカニズムの理解を深化させるため、脳実質に加え、近年その機能的重要性が注目させつつある脳境界を標的とした解析を進め、脳機能低下メカニズムの統合的な理解を目指しています。単純な細胞個々の解析にとどまらず、多細胞種間、さらには脳境界を含めた領域間や末梢との関係に至る様々なスケールで解析を進め、脳機能の低下に至る分子基盤の理解ならびに脳実質・境界領域の機能・構造変容を標的とした介入技術の開発・検証を進めています。
総説
Yamamoto S, Masuda T. Lipid in microglial biology – from material to mediator. Inflamm Regen. 43(1):38, 2023. doi: 10.1186/s41232-023-00289-z.
Amann L, Masuda T, Prinz M. Mechanisms of myeloid cell entry to the healthy and diseased central nervous system. Nat Immunol. 24(3):393-407, 2023. doi: 10.1038/s41590-022-01415-8.
主な論文業績
Yamasaki A, Shintaku H, Harada A, Maehara K, Tanaka K, Saeki M, Ito M, Konishi H, Tsuda M, Prinz M, Kishi Y, Ohkawa Y, Yamamoto S, Masuda T. Cyclin-dependent kinase inhibitor 1A mediates mouse line- and fate-dependent cellular responses in Cx3cr1-Cre genetic tools. Cell Rep.44(9):116267, 2025. doi: 10.1016/j.celrep.2025.116267.
Frosch M, Shimizu T, Wogram E, Amann L, Gruber L, Groisman AI, Fliegauf M, Schwabenland M, Chhatbar C, Zechel S, Rosewich H, Gärtner J, Quintana FJ, Buescher JM, Blank T, Binder H, Stadelmann C, Letzkus JJ, Hopf C, Masuda T, Knobeloch KP, Prinz M. Microglia-neuron crosstalk through Hex-MG2-MGL2 mains brain homeostasis. Nature. 646(8086):913-924, 2025. doi: 10.1038/s41586-025-09477-y.
Yamasaki A, Imanishi I, Tanaka K, Ohkawa Y, Tsuda M, Masuda T. IRF8 and MAFB drive distinct transcriptional machineries in different resident macrophages of the central nervous system. Commun Biol. 7(1):896, 2024. doi: 10.1038/s42003-024-06607-6.
Masuda T, Amann L, Monaco G, Sankowski R, Staszewski O, Krueger M, Del Gaudio F, He L, Paterson N, Nent E, Fernández-Klett F, Yamasaki A, Frosch M, Fliegauf M, Bosch LFP, Ulupinar H, Hagemeyer N, Schreiner D, Dorrier C, Tsuda M, Grothe C, Joutel A, Daneman R, Betsholtz C, Lendahl U, Knobeloch KP, Lämmermann T, Priller J, Kierdorf K, Prinz M. Specification of CNS macrophage subsets occurs postnatally in defined niches. Nature. 604(7907):740-748, 2022. doi: 10.1038/s41586-022-04596-2.
Masuda T, Amann L, Sankowski R, Staszewski O, Lenz M, D Errico P, Snaidero N, Costa Jordão MJ, Böttcher C, Kierdorf K, Jung S, Priller J, Misgeld T, Vlachos A, Meyer-Luehmann M, Knobeloch KP, Prinz M. Novel Hexb-based tools for studying microglia in the CNS. Nat Immunol. 21(7):802-815, 2020. doi: 10.1038/s41590-020-0707-4.
Masuda T, Sankowski R, Staszewski O, Böttcher C, Amann L, Sagar, Scheiwe C, Nessler S, Kunz P, van Loo G, Coenen VA, Reinacher PC, Michel A, Sure U, Gold R, Grün D, Priller J, Stadelmann C, Prinz M. Spatial and temporal heterogeneity of mouse and human microglia at single-cell resolution. Nature. 566(7744):388-392, 2019. doi: 10.1038/s41586-019-0924-x.