研究室リンク
専門分野
生体光物理、量子生命科学、ナノフォトニクス
研究概要
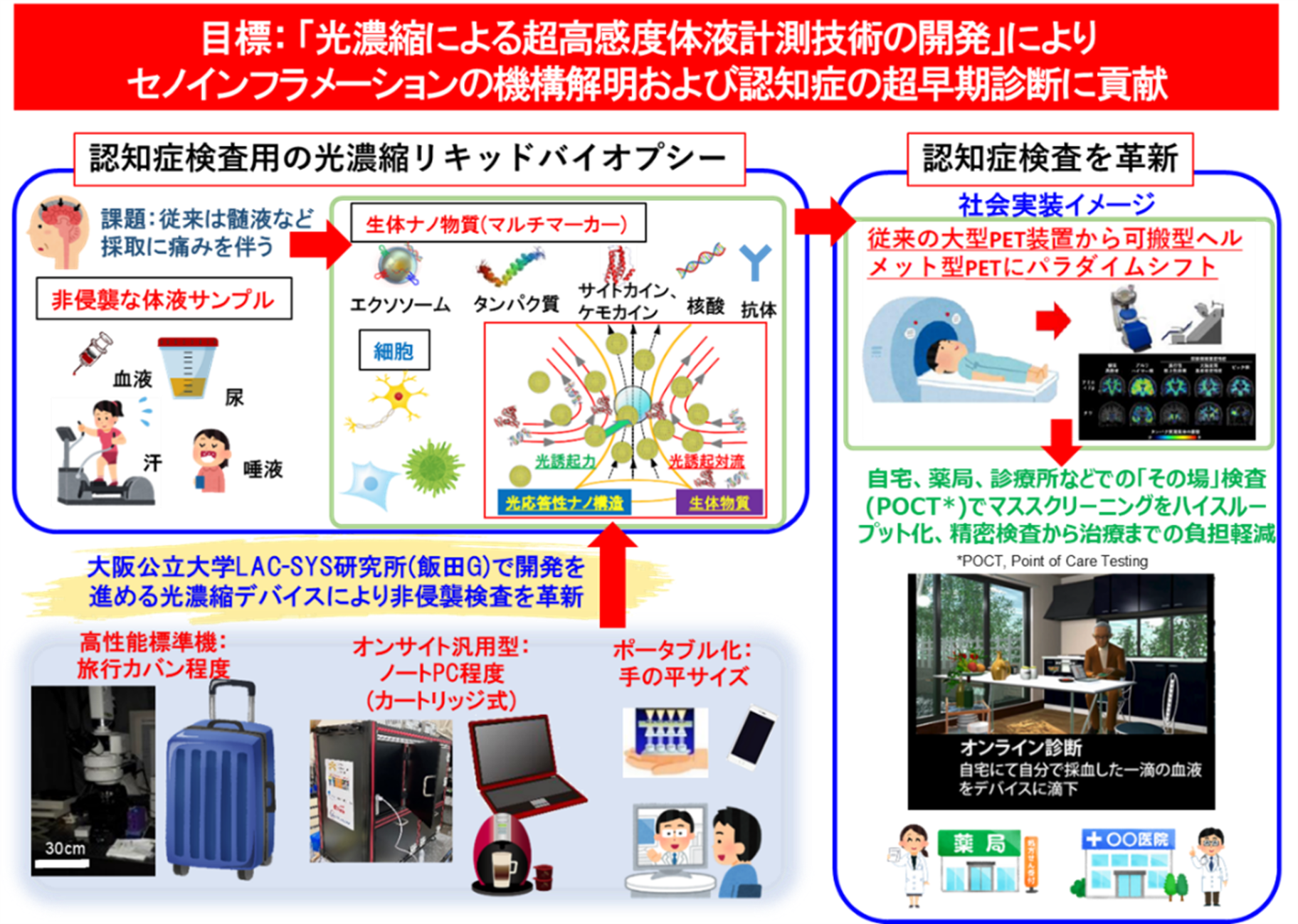
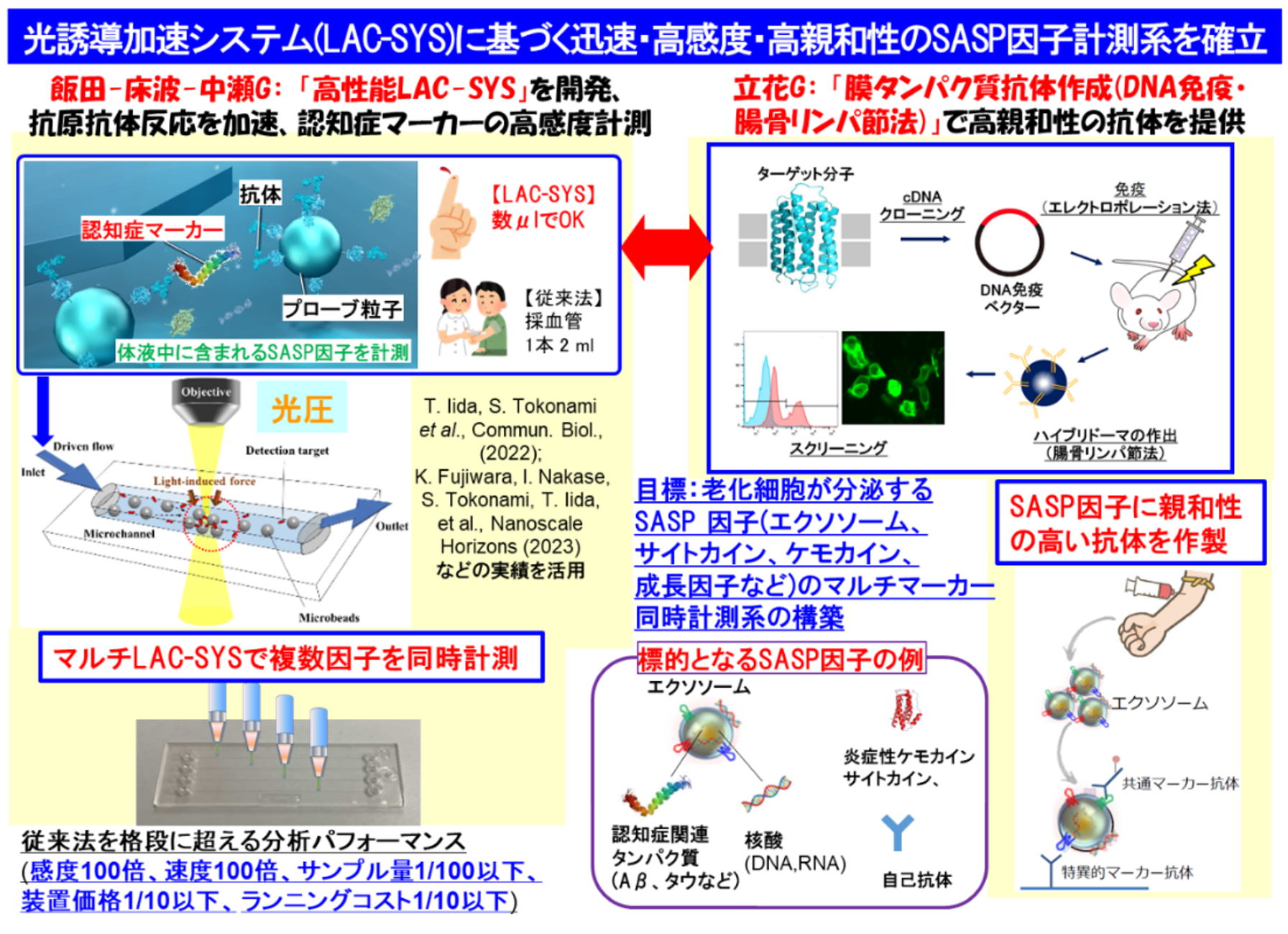
「光濃縮チーム」では光濃縮による超高感度認知症マーカー計測技術の開発を担当し、血液中の認知症マーカーの超高感度計測に向けて光濃縮検査システムのハードウェア最適化を推進します。これまで、飯田らは光圧と光誘起対流の相乗効果により標的物質を光濃縮して抗原抗体反応などの生化学反応を加速する光誘導加速システム(LAC-SYS)を開発してきました。たとえば、数百nLの極微量液体試料からアトグラムレベル(10-18 g)の微量タンパク質の計測を3~5分で可能とするマイクロフローLAC-SYS[Commun. Biol 2022]や、5分以内で簡便に抗体修飾や高感度・迅速計測ができるナノボウル光濃縮基板[npj Biosensing 2024]などの技術を駆使し、細胞老化随伴分泌現象(SASP)因子と呼ばれる老化細胞由来のエクソソーム、サイトカイン、ケモカイン、成長因子などの計測系構築を実施します。薬剤による細胞若返りや老化促進因子のブロックによる疾患予防に向け、大阪公立大学メンバー(研究協力者: 床波志保、中瀬生彦、立花太郎)と協力して要素技術となる基板開発、抗体開発を推進しながら、高性能標準機の感度・迅速性に匹敵し、安価かつ容易に体液中マーカーの測定結果が得られる普及型の光濃縮検査システムを開発して本プロジェクトに貢献します。
主な研究内容
光誘導加速システム(LAC-SYS)の高性能標準機による老化細胞由来マーカー計測
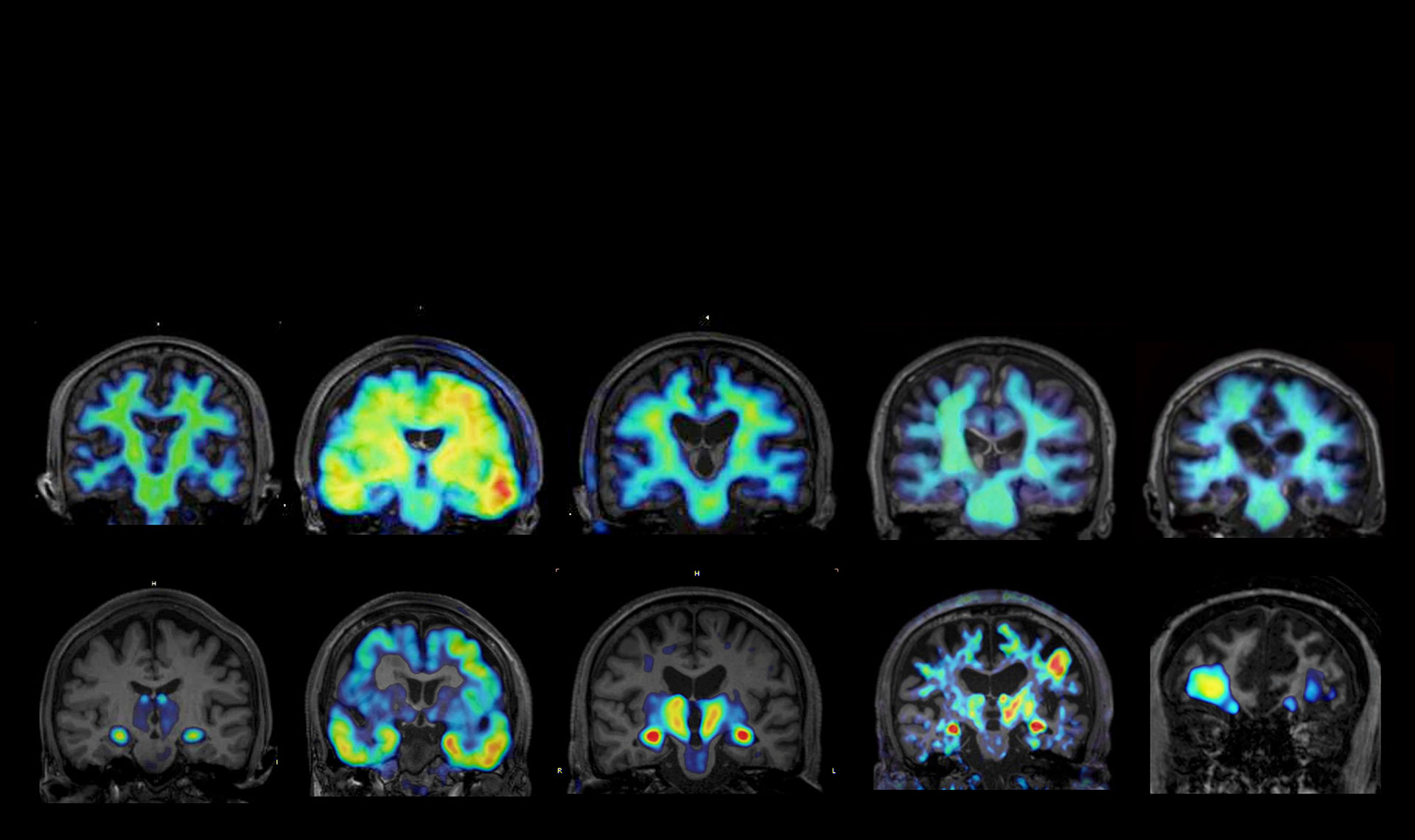
これまでに開発してきたマイクロフローLAC-SYSやナノボウル光濃縮基板を駆使し、凝集性タンパク質、エクソソーム、サイトカインなどを標的とし、認知症マーカー凝集性タンパクやSASP 因子の高感度・迅速な計測な計測を可能とするアッセイの構築を推進します。また、従来分析装置(免疫測定など)との比較・融合により老化細胞中上清や体液中の成分分析を簡易に行える環境構築も目指します。さらに、LAC-SYSに最適化された高特異性・高親和性のSASP因子用の抗体作製・改良も行います。また、代表者の樋口グループにおけるPETや従来型の免疫測定法による測定結果との比較を中心に、複数医療機関で測定した患者由来体液サンプルにおける測定値と認知症の病態との相関の解明をAIなどDX技術との融合により目指します。これらの取組により、高診断精度での認知症の超早期発見のためのプラットフォームの構築に貢献します。
体液中SASP因子計測用LAC-SYSの試作機開発と医療機関への実装・普及
医療現場で簡便に利用できるポータブル光濃縮システムに基づく普及型LAC-SYSを開発し、体液中SASP因子を標的とする光誘導イムノアッセイの条件探索を進めます。具体的には、高性能LAC-SYSと普及型LAC-SYS試作機の各測定データの相関を取りながら光学系とフロー系の最適化を行い、マルチマーカー測定ができる試作機の開発を進めます。特に、老化細胞由来のエクソソームとサイトカイン、ケモカインや成長因子などの計測および、これらに適合した高特異性・高親和性の抗体作製もフィードバックをかけながら進め、複数検体を高再現性で同時に測定できる光学系の構築や、光濃縮バイオチップの改良・組成分析を行い、大阪健康長寿医科学センター(大阪長寿)など参画医療機関への設置による大規模コホートでの臨床サンプル測定に向けた研究開発を推進します。
研究内容をまとめた総説
- T. Iida*, “Development of Innovative Bio-Measurement Technology by Micro-Flow Light-Induced Acceleration”, READOUT Horiba Technical Report., 55, 11 (2021).
- T. Iida*, “Applications and prospects of light-induced acceleration systems for medical, food, and environmental measurements”, Oyo Buturi < Perspective >, 94 (5), 244 (2025).
- Shiho Tokonami*, Takuya Iida*, "Review: Novel Sensing Strategies for Bacterial Detection Based on Active and Passive Methods Driven by Ext Macroscopically Anisotropic Structures Produced by Light-induced Solvothermal Assembly of Porphyrin Dimers ernal Field", Analytica Chimica Acta, Vol.988, 1-16. (2017).
- 飯田琢也、床波志保、伊都将司、「光と揺らぎによるナノ物質の動態制御と生体模倣エンジニアリング」、光学、Vol.46, No.3, 104-112, 2017.
主な論文業績
- K. Hayashi, M. Tamura, M. Fujiwara, S. Tokonami*, T. Iida*, “Highly efficient three-dimensional optical condensation of nano- and micro-particles using a gold-coated optical fibre module”, Communications Physics, 9, 68 (2026).
- S. Toyouchi, S. Oomachi, R. Hasegawa, K. Hayashi, Y. Takagi, M. Tamura, S. Tokonami,* T. Iida*, “Single Nucleotide Polymorphism Highlighted via Heterogeneous Light-Induced Dissipative Structure”, ACS Sensors, 10, 751 (2025).
- M. Kanoda, K. Hayashi, Y. Takagi, M. Tamura, S. Tokonami*, T. Iida*, “High-throughput Light-induced Immunoassay with Milliwatt-level Laser under One-minute Optical Antibody-coating on Nanoparticle-imprinted Substrate”, npj Biosensing, 1, 1, (2024).
- K. Fujiwara, Y. Takagi, M. Tamura, M. Omura, K. Morimoto, I. Nakase*, S. Tokonami*, T. Iida*, “Ultrafast Sensitivity-Controlled and Specific Detection of Extracellular Vesicles Using Optical Force with Antibody-modified Microparticles in a Microflow System”, Nanoscale Horizons, 8, 1034-1042 (2023).
- I. Nakase*, M. Miyai, K. Noguchi, M. Tamura, Y. Yamamoto, Y. Nishimura, M. Omura, K. Hayashi, S. Futaki, S. Tokonami*, T. Iida*, “Light-Induced Condensation of Biofunctional Molecules around Targeted Living Cells to Accelerate Cytosolic Delivery”, Nano Letters, 22, 24, 9805–9814. (2022).
- T. Iida*, S. Hamatani, Y. Takagi, K. Fujiwara, M. Tamura, S. Tokonami, “Attogram-level light-induced antigen-antibody binding confined in microflow”, Communications Biology, 5, 1053 (2022).
- M. Tamura, T. Iida, K. Setoura*, “Plasmonic nanoscale temperature shaping on a single titanium nitride nanostructure”, Nanoscale, 14, 12589-12594 (2022).
- K. Hayashi, Y. Yamamoto, M. Tamura, S. Tokonami*, T. Iida*, “Damage-free Light-induced Assembly of Intestinal Bacteria with a Bubble-mimetic Substrate”, Communications Biology, 4, 385 (2021).
- S. Tokonami*, S. Kurita, R. Yoshikawa, K. Sakurai, T. Suehiro, Y. Yamamoto, M. Tamura, O. Karthaus, T. Iida*, “Light-induced assembly of living bacteria with honeycomb substrate”. Science Advances, 6, eaaz5757 (2020).
- M. Tamura*, T. Omatsu, S. Tokonami, T. Iida*, "Interparticle-interaction-mediated Anomalous Acceleration of Nanoparticles under Light-field with Coupled Orbital and Spin Angular Momentum", Nano Letters, 2019, 19, 8, 4873-4878 (2019).
- Y. Yamamoto, S. Tokonami*, T. Iida*, “Surfactant-Controlled Photothermal Assembly of Nanoparticles and Microparticles for Rapid Concentration Measurement of Microbes”, ACS Applied Bio Materials, 2, 1561–1568 (2019).
- M. Ueda, Y. Nishimura, M. Tamura, S. Ito, S. Tokonami*, T. Iida*, "Microflow-mediated optical assembly of nanoparticles with femtogram protein via shrinkage of light-induced bubbles", APL Photonics, 4, 010802 (2019).
- T. Iida*, Y. Nishimura, M. Tamura, K. Nishida, S. Ito, S. Tokonami*, “Submillimetre Network Formation by Light-induced Hybridization of Zeptomole-level DNA”, Scientific Reports, 6, 37768(1-9) (2016).
- Y. Nishimura, K. Nishida, Y. Yamamoto, S. Ito, S. Tokonami*, T. Iida*, “Control of Submillimeter Phase Transition by Collective Photothermal Effect”, J. Phys. Chem. C; 118, 18799-18804 (2014).