研究室リンク
専門分野
ケミカルバイオロジー
研究概要
ムーンショット目標7「グリア病態からセノインフラメーションへ発展する概念に基づく認知症発症機序の早期検出と制御」において、研究分担者として、動物個体における神経細胞およびグリア細胞の内在性表層受容体の非侵襲・細胞種選択的な可視化および活性制御技術の開発を担当します。本研究を通じて、脳変性疾患の本質的理解と、受容体レベルに立脚した革新的介入技術の創出を目指します。
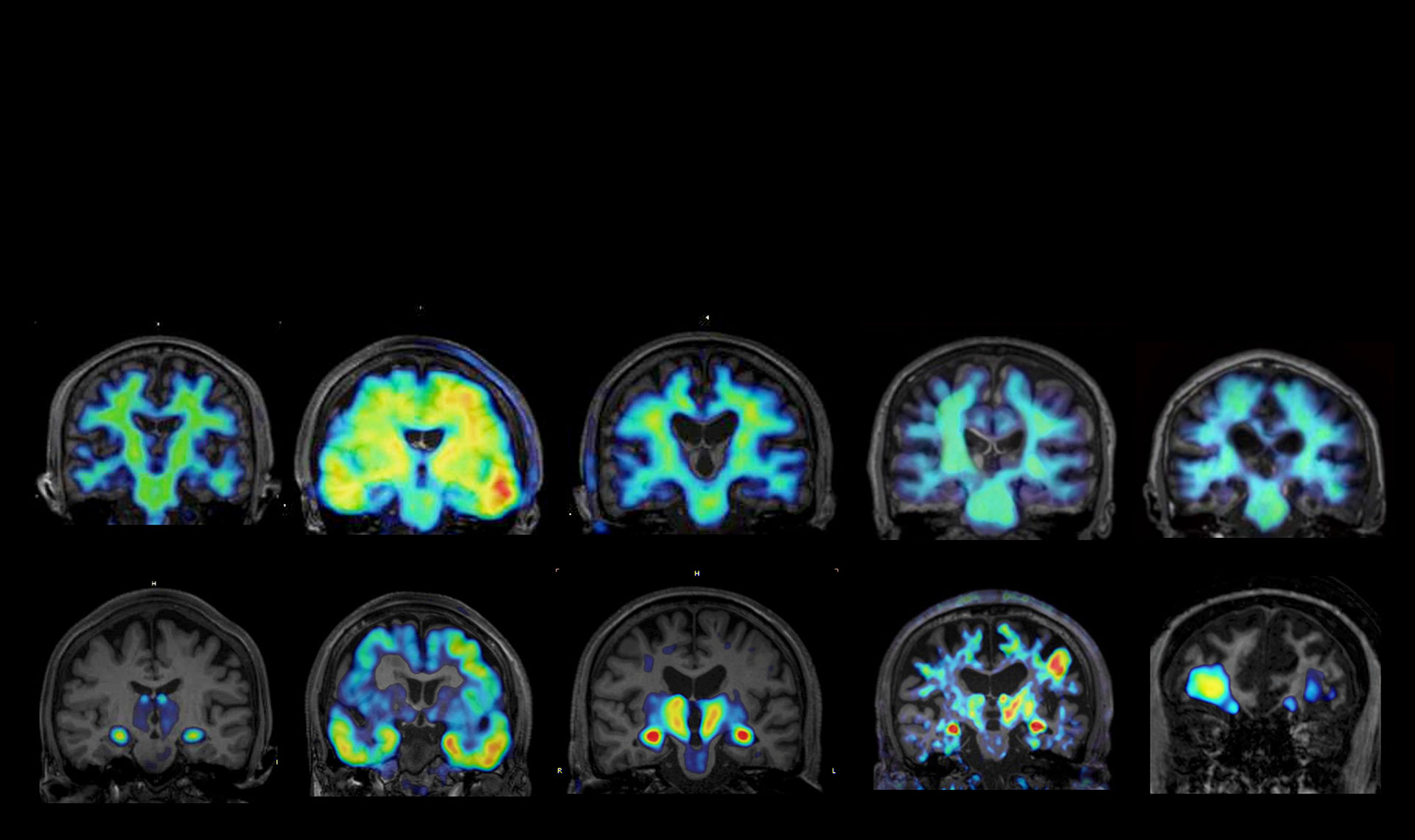
近年、蛍光タンパク質技術の進展により、細胞内タンパク質の動態可視化は広く普及しました。しかしその多くは、内在性タンパク質に対して融合タンパク質を過剰発現させる手法に依存しており、生理的発現量や本来の分子挙動を必ずしも正確に反映していません。細胞内タンパク質の発現量や局在は厳密に制御されていることから、生理状態および病態における真の分子動態を捉えるためには、内在性タンパク質を直接可視化する技術の確立が不可欠です。これまで私たちは、神経細胞に内在する神経伝達物質受容体を対象に、内在性受容体の可視化技術を開発してきました。本研究ではこれをさらに発展させ、グリア細胞に内在する受容体をin vivoで高精度に可視化する技術へと展開します。これにより、認知症をはじめとする神経変性疾患において生じる細胞機能の異常を、高い時間・空間分解能で捉えることを目指します。
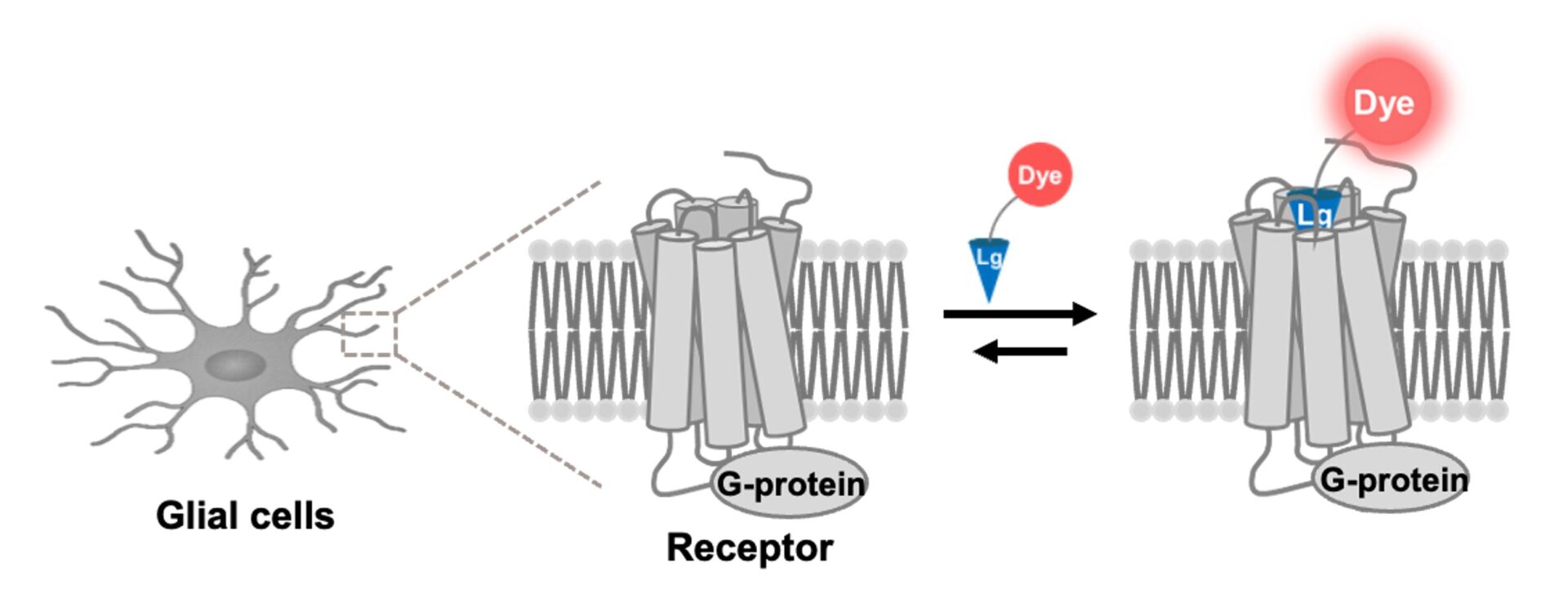
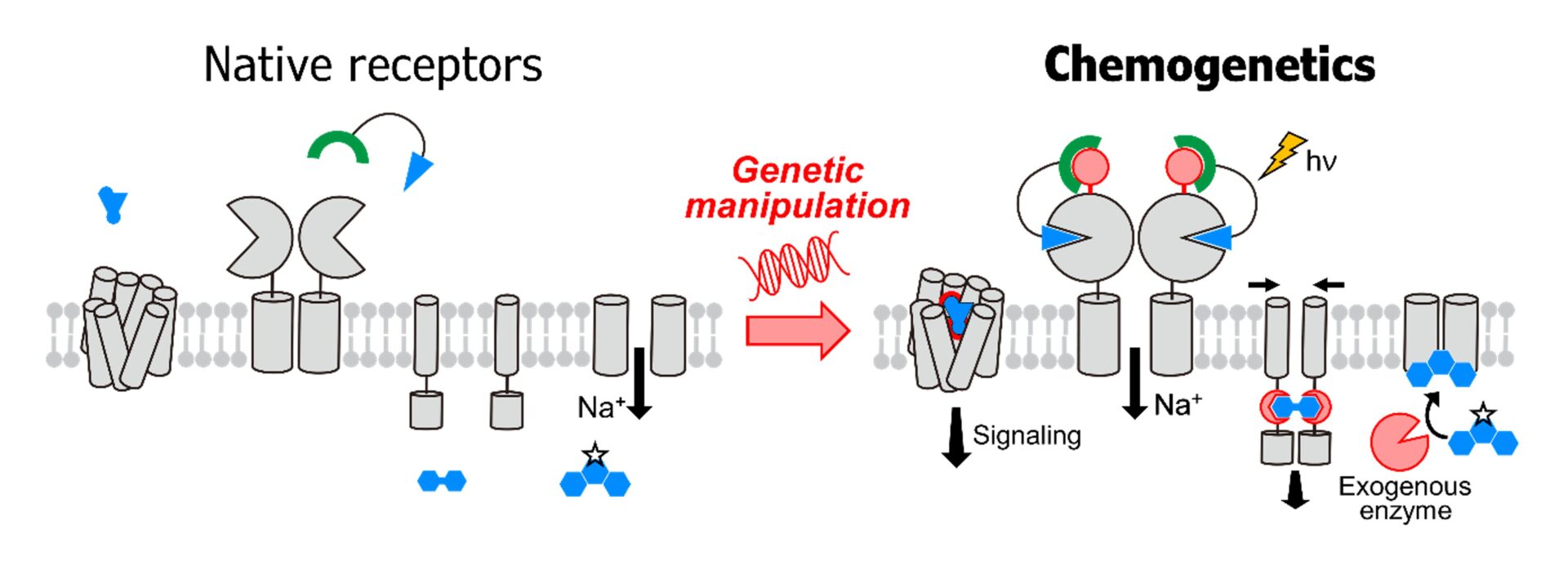
近年、光遺伝学(オプトジェネティクス)や化学遺伝学(ケモジェネティクス)の発展により、特定細胞の活動を任意のタイミングで操作する技術が確立され、脳回路研究に不可欠なツールとなっています。しかし、これらの多くは神経活動などを人工的に操作するものであり、細胞に内在する個々のタンパク質機能を直接解明する手法としては適用が困難です。本研究では、細胞種選択的に、内在性受容体の活性を任意のタイミングで選択的かつ可逆的に阻害する新たな受容体制御技術を開発します。本技術は、受容体の生理機能解明に資するだけでなく、標的選択性の高い介入を可能とすることから、副作用を低減した次世代創薬への応用も期待されます。
主な研究内容
神経変性疾患時の神経細胞・グリア細胞の変容を捉える可視化プローブの開発
これまで私たちは、AMPA型グルタミン酸受容体の可視化プローブを開発し、培養神経細胞において神経活動に伴うシナプスAMPA受容体動態の変化を明らかにしてきました。本研究では、これらのプローブを神経変性疾患時のシナプス変容を捉えるツールとして位置づけ、名古屋大学・和氣弘明らとの連携によるin vivo多光子イメージングを通じて、マウス脳内での可視化技術へと発展させます。さらに、グリア細胞の変容を可視化するプローブの開発を進めます。具体的には、ミクログリアやアストロサイトなど、各グリア細胞に特異的な表層マーカータンパク質を標的とした可視化プローブを設計し、和氣らとの連携によるin vivoイメージングによって脳内グリア細胞の動態を高精度に捉える技術を確立します。加えて、多光子イメージングに最適化した高感度・高分解能蛍光プローブの開発を進め、受容体動態の詳細な解析を可能にします。また、受容体を標的とするMRIプローブの開発にも取り組み、受容体分解能で脳深部の病態変容を捉える新たな可視化技術の確立を目指します。
細胞種選択的介入操作による脳疾患時の受容体機能解明
本研究では、細胞種選択的な介入操作により、神経変性疾患におけるグリア細胞および受容体機能の解明を目指します。これまでに私たちは、受容体本来の機能を保持したまま、化学物質による制御能を付与する独自の手法を開発してきました。この手法は、既存のDREADDなどの化学遺伝学とは異なり、細胞活動全体を操作するのではなく、内在性受容体そのものの活性を人為的に制御できる点に特徴があります。従来の多くの手法が受容体活性の「人為的活性化」に主眼を置いていたのに対し、本研究では、遺伝子改変と化学的手法を組み合わせた独自の化学遺伝学により、標的受容体機能を細胞選択的かつ可逆的に「阻害」する技術の開発を行います。これにより、動物個体内で、狙った細胞種における特定受容体の活性を、任意のタイミングで精密に抑制することが可能となります。本手法を脳疾患モデルに適用することで、各種グリア細胞における受容体機能の役割を明確化するとともに、遺伝子工学と薬理学を融合した次世代創薬プラットフォームとしての可能性を追求していきます。
研究開発分担者の主な論文業績
- Soga K., Fujiwara T., Nakagawa M., Shibata A., Adriel H., Yatsuzuka K., Kakegawa W., Yuzaki M., Hamachi I., Nango E., Kiyonaka S. Rapid and reversible fluorescent probe enables repeated snapshot imaging of AMPA receptors during synaptic plasticity. Sci. Adv., 11, eadt6683 (2025). DOI: 10.1126/sciadv.adt6683
- Suzuki H., Doura T., Matsuba Y., Matsuoka Y., Araya T., Asada H., Iwata S., Kiyonaka S. Photoresponsive adenosine derivatives for the optical control of adenosine A2A receptor in living cells. ACS Chem. Biol. 19, 2494-2501 (2024) DOI: 10.1021/acschembio.4c00583.
- Nonaka H., Sakamoto S., Shiraiwa K., Ishikawa M., Tamura T., Okuno K., Kondo T., Kiyonaka S., Susaki E.A., Shimizu C., Ueda H.R., Kakegawa W., Arai I., Yuzaki M., Hamachi I. Bioorthogonal chemical labeling of endogenous neurotransmitter receptors in living mouse brains. Proc. Natl. Acad. Sci. USA, 121, e2313887121 (2024) DOI: 10.1073/pnas.2313887121
- Ojima K., Kakegawa W., Yamasaki T., Miura Y., Itoh M., Michibata Y., Kubota R., Doura T., Miura E., Nonaka H., Mizuno S., Takahashi S., Yuzaki M., Hamachi I., Kiyonaka S. Coordination chemogenetics for activation of GPCR-type glutamate receptors in brain tissue. Nat. Commun., 13, 3167 (2022). DOI: 10.1038/s41467-022-30828-0
- Ojima K., Shiraiwa K., Soga K., Doura T., Takato M., Komatsu K., Yuzaki M., Hamachi I., Kiyonaka S. Ligand-directed two-step labeling to quantify neuronal glutamate receptor trafficking. Nat. Commun., 12, 831 (2021). DOI: 10.1038/s41467-021-21082-x.
- Wakayama S., Kiyonaka S., Arai I., Kakegawa W., Matsuda S., Ibata K., Nemoto L.Y., Kusumi A., Yuzaki M., Hamachi I. Chemical labeling for visualizing native AMPA receptors in live neurons. Nat. Commun., 8, 14850 (2017). DOI: 10.1038/ncomms14850.
- Kiyonaka S., Kubota R., Michibata Y., Sakakura M., Takahashi H., Numata T., Inoue R., Yuzaki M., Hamachi I. Allosteric activation of membrane-bound glutamate receptors using coordination chemistry within living cells. Nat. Chem., 8, 958-967 (2016). DOI: 10.1038/nchem.2554.